03/03/2024 • 28 min de leitura
Atualizado em 31/07/2025Sistema imunológico: Doenças autoimunes
O Que é o Sistema Imunológico e Por Que Ele é Tão Importante?
O sistema imunológico, também conhecido como sistema imune ou sistema de defesa, é a complexa rede de estruturas e processos biológicos do nosso organismo, cuja principal função é a proteção contra doenças. Ele atua como um verdadeiro "guarda-costas", defendendo-nos contra uma vasta gama de agentes agressores, como vírus, bactérias, parasitas, fungos e até mesmo células do próprio corpo que se tornam alteradas, como as células malignas (tumorais). A capacidade de distinguir entre o "próprio" (o que faz parte do nosso corpo) e o "não-próprio" (o que é estranho e potencialmente perigoso) é a base fundamental para o seu funcionamento correto.
A ciência da imunologia, que estuda todos os aspectos do sistema imunológico, teve um de seus marcos com Ilya Ilyich Mechnikov, considerado o pai da imunologia, em 1882. Ao longo do século XX, os avanços na compreensão dos processos biológicos revolucionaram a saúde, levando à erradicação de doenças, redução da mortalidade e aumento da expectativa de vida. Atualmente, em sociedades desenvolvidas, as doenças crônicas, incluindo as doenças autoimunes, representam as principais ameaças à vida e à qualidade de vida.
Mas, o que acontece quando esse guardião, o sistema imunológico, falha? Em vez de proteger, ele pode erroneamente atacar o próprio corpo, dando origem às doenças autoimunes.
Imunidade Inata: A Primeira Linha de Defesa (Não Específica)
A imunidade inata, também chamada de não específica, é a primeira e mais rápida linha de defesa do nosso organismo. Ela está constitutivamente presente e pronta para ser mobilizada imediatamente após a detecção de um invasor. Diferente da imunidade adaptativa, a inata não é específica para um antígeno e reage da mesma forma a uma variedade de organismos, não possuindo memória imunológica. É um sistema de defesa ancestral, encontrado desde organismos unicelulares até os mais complexos.
Seus componentes podem ser divididos em barreiras:
1. Barreiras Físicas e Mecânicas:
São as primeiras a impedir a entrada de patógenos.
Pele: Atua como uma barreira física quase impermeável à maioria dos agentes infecciosos. Sua descamação natural ajuda a remover bactérias e outros invasores.
Membranas Epiteliais Internas: Revestem órgãos como pulmões, intestino, trato genitourinário, estômago e nariz.
Movimentos Mecânicos:
Tosse e Espirros: Expelir mecanicamente patógenos do trato respiratório.
Fluxo de Lágrimas e Saliva: Lavam e removem patógenos dos olhos e boca.
Muco: Secretado pelos tratos respiratório e digestivo, retém microrganismos.
Peristalse Intestinal e Cílios Bronco-Pulmonares: Movimentos que mantêm as vias aéreas e o trato gastrointestinal livres de organismos.
2. Barreiras Químicas:
Atuam quando as barreiras físicas são penetradas.
Peptídeos Antimicrobianos: Como as β defensinas, secretadas pela pele e trato respiratório.
Enzimas Antissépticas:
Lisozima: Presente na saliva e leite materno, degrada a parede celular bacteriana.
Fosfolipase A2: Presente na saliva.
Acidez: Baixo pH do suor e da secreção gástrica previnem o crescimento bacteriano. Secreções vaginais também são ácidas.
Sistema Complemento: Uma cascata bioquímica de mais de vinte proteínas, o principal mecanismo de defesa humoral não específico. Quando ativado, ele:
Aumenta a permeabilidade vascular.
Recruta células fagocitárias.
Promove a lise (ruptura) e opsonização (marcar para destruição) de bactérias.
Sistema de Coagulação: Alguns de seus produtos contribuem para a defesa imune, aumentando a permeabilidade vascular e agindo como agentes quimiotáxicos (atraindo células). Beta-lisina, uma proteína produzida pelas plaquetas, pode lisar bactérias Gram-positivas.
Lactoferrina e Transferrina: Limitam o crescimento bacteriano ao ligarem-se ao ferro, nutriente essencial para bactérias.
Interferons: Proteínas que limitam a replicação de vírus nas células.
Interleucina-1 (IL-1): Induz febre e a produção de proteínas de fase aguda, algumas das quais opsonizam bactérias.
3. Barreiras Celulares:
Constituem a segunda linha de defesa da imunidade inata, agindo quando os patógenos penetram os tecidos. Os principais tipos celulares são:
Leucócitos (Glóbulos Brancos):
Fagócitos: Células que englobam (fagocitam) e destroem patógenos ou partículas. Patrulham o corpo ou são recrutados por citocinas.
Neutrófilos (PMNs): Os mais abundantes, chegam rapidamente ao local da infecção, fagocitam invasores e os matam intracelularmente. Contribuem para lesões colaterais durante a inflamação.
Macrófagos: Células versáteis nos tecidos, fagocitam e matam microrganismos. Atuam como necrófagos (eliminando células mortas e detritos) e como Células Apresentadoras de Antígenos (APCs), cruciais para ativar a imunidade adaptativa.
Células Dendríticas: Encontradas em tecidos de contato com o ambiente externo (pele, pulmões, intestinos), ligam a imunidade inata e adaptativa, apresentando antígenos aos linfócitos T.
Células Natural Killer (NK): Linfócitos que atacam e destroem células tumorais ou células infectadas por vírus de forma não específica. Elas distinguem células normais de alteradas pela presença ou ausência de moléculas MHC classe I na superfície da célula alvo.
Eosinófilos: Contêm proteínas eficientes na destruição de certos parasitas.
Mastócitos: Presentes no tecido conjuntivo e mucosas, regulam a resposta inflamatória e estão associados a alergias. Liberam mediadores químicos como a histamina, que causa vasodilatação, calor e atração de leucócitos.
Receptores de Reconhecimento de Padrões (PRRs): Encontrados na superfície ou interior das células imunes inatas, reconhecem PAMPs (Padrões Moleculares Associados a Patógenos) e DAMPs (Padrões Moleculares Associados a Danos), permitindo a identificação genérica de invasores. Exemplos: Receptores Semelhantes a Toll (TLRs), Receptores Semelhantes a Nod (NLRs), Receptores Semelhantes a Rig (RLRs).
4. Resposta Inflamatória:
É uma das primeiras reações do sistema imunológico à infecção. Caracteriza-se por vermelhidão, inchaço, calor e dor localizada. É mediada por eicosanoides (prostaglandinas, leucotrienos) e citocinas (interleucinas, quemoquinas, interferons), que recrutam células imunes e promovem a cura do tecido danificado.
Imunidade Adaptativa: A Resposta Específica com Memória
A imunidade adaptativa, ou específica, é o segundo nível de defesa dos vertebrados e é ativada pela resposta inata. Seu grande diferencial é a capacidade de se adaptar para reconhecer eficientemente agentes patogênicos específicos e, o mais importante, criar memória imunológica. Isso permite que, em um novo contato com o mesmo patógeno, a resposta seja mais rápida e robusta.
1. Discriminação "Próprio" vs. "Não-Próprio":
O sistema adaptativo distingue proteínas produzidas pelo próprio corpo ("self") de proteínas de invasores ("non-self"). Essa distinção é feita por receptores de superfície altamente diversos nos linfócitos:
TCRs (Receptores de Células T)
BCRs (Receptores de Células B), que são anticorpos presos à membrana A variabilidade praticamente ilimitada desses receptores é alcançada por processos únicos de recombinação genética e mutação acelerada, permitindo ao sistema imunológico criar anticorpos contra quase qualquer molécula.
2. Tolerância Imunológica:
Durante o desenvolvimento, no timo (para linfócitos T) e na medula óssea (para linfócitos B), células especializadas apresentam aos jovens linfócitos as moléculas do próprio organismo. Todos os linfócitos que reagem a essas moléculas "próprias" são destruídos, garantindo que apenas os linfócitos indiferentes ao próprio (e mais propensos a reagir ao não-próprio) sejam liberados na corrente sanguínea. Esse processo é essencial para prevenir a autoimunidade.
3. Células de Memória:
Quando um linfócito encontra um antígeno para o qual seu receptor é específico, ele é estimulado, multiplica-se e gera células efetoras e células de memória. As células de memória são de vida longa, quiescentes, e permitem que o organismo responda mais rapidamente e com maior intensidade a infecções futuras pelo mesmo agente.
4. Tipos de Linfócitos e Suas Funções:
Os linfócitos são os principais efetores do sistema imunitário específico.
Linfócitos B (Células B):
Possuem um BCR (anticorpo preso à membrana) específico.
Concentram-se nos gânglios linfáticos, onde filtram a linfa e esperam encontrar um antígeno "não-próprio".
Ao se ligarem a um antígeno específico e serem estimuladas por citocinas de Linfócitos T CD4+, multiplicam-se e diferenciam-se em:
Plasmócitos: Produtoras de grandes quantidades de anticorpos solúveis (não presos à membrana), específicos para aquele antígeno.
Células B de Memória: Para respostas futuras mais rápidas.
Anticorpos: Proteínas receptoras livres no sangue que se ligam a moléculas "não-self". Eles atuam de várias formas:
Neutralização: Cobrem a superfície de vírus ou bactérias, impedindo sua ligação às células hospedeiras.
Opsonização: Atraem fagócitos ao marcarem o invasor.
Ativação do Sistema Complemento: Levam à lise do patógeno.
Estimulação de Células Citotóxicas: Para destruir células identificadas pelo anticorpo.
Tipos de Anticorpos: IgM (primeiro a ser produzido), IgG (principal no sangue, alta afinidade), IgA (nas mucosas), IgE (parasitoses, alergias), IgD (estimula o sistema imunológico).
Linfócitos T (Células T):
Linfócitos T CD8+ (Citotóxicos ou Killers):
Possuem um TCR específico em sua membrana.
Reconhecem células humanas (infectadas por vírus ou tumorais) que apresentam peptídeos "não-self" em moléculas MHC Classe I na sua superfície.
Após o reconhecimento e, em geral, estimulação por citocinas de linfócitos T CD4+, liberam substâncias como perforinas (criam poros e causam lise) ou granzimas (induzem apoptose – morte celular programada) para destruir a célula alvo.
Formam células T CD8+ de memória para respostas futuras mais eficientes.
Linfócitos T CD4+ (Auxiliares ou Helpers):
São os controladores de toda a resposta imunitária.
Possuem TCRs que se ligam a peptídeos apresentados em moléculas MHC Classe II por Células Apresentadoras de Antígenos (APCs).
Após o reconhecimento, liberam citocinas que ativam ou inibem outras células imunitárias. A falha dos T4 (como na AIDS/SIDA) leva ao colapso do sistema imune.
Dois tipos principais de resposta TH (Helper T):
TH1: Produz citocinas como IL-2, IFN-gama e TNF-beta. Ativa macrófagos e mecanismos citotóxicos, eficaz contra patógenos intracelulares (vírus, bactérias intracelulares).
TH2: Secreta IL-4 e IL-5. Estimula a produção de anticorpos pelos linfócitos B, eficaz contra organismos extracelulares (bactérias, parasitas).
Linfócitos T Reguladores (Supressores): Limitam e suprimem reações imunitárias, prevenindo danos excessivos ao corpo. Descobertas recentes indicam que as células B no timo podem educar as células T para não atacarem os tecidos do corpo. Interrupções nesse processo podem ser gatilhos para distúrbios autoimunes.
5. Citocinas:
São as "hormônios" do sistema imunitário, permitindo que as células se comuniquem entre si e com outros órgãos. São um sistema complexo com funções como:
IL-1: Causa febre, tremores, mal-estar; promove inflamação; estimula linfócitos T.
IL-2: Estimula multiplicação de linfócitos T e B.
IL-4, IL-5, IL-6: Estimulam linfócitos B e produção de anticorpos.
IFN-alfa: Ativa "alerta viral" nas células, inibe produção de proteínas virais.
IFN-gama: Ativa macrófagos, tornando-os mais eficientes e agressivos; promove inflamação; estimula resposta TH1.
TNF-alfa (Fator de Necrose Tumoral): Induz secreção de citocinas, responsável por perda de peso em inflamação crônica; ativa fagócitos, estimula resposta citotóxica (TH1).
Desordens do Sistema Imunológico: O Que Acontece Quando Ele Falha?
O sistema imune, apesar de sua notável complexidade, pode apresentar falhas que levam a transtornos categorizados em imunodeficiências, hipersensibilidades e, nosso foco principal, autoimunidade.
1. Imunodeficiências:
Ocorrem quando a atividade do sistema imunológico é inferior ao normal, resultando em infecções recorrentes e risco de vida. Podem ser causadas por fatores genéticos, doenças adquiridas (como HIV/AIDS), má nutrição, alcoolismo, uso de drogas e o próprio envelhecimento (imunossenescência).
2. Hipersensibilidade:
Uma resposta imunitária excessiva que danifica os próprios tecidos do corpo. Existem quatro tipos (I a IV), incluindo reações anafiláticas (alergias) e reações mediadas por anticorpos ou células que atacam tecidos próprios.
3. Doenças Autoimunes: Quando o Corpo Ataca a Si Mesmo
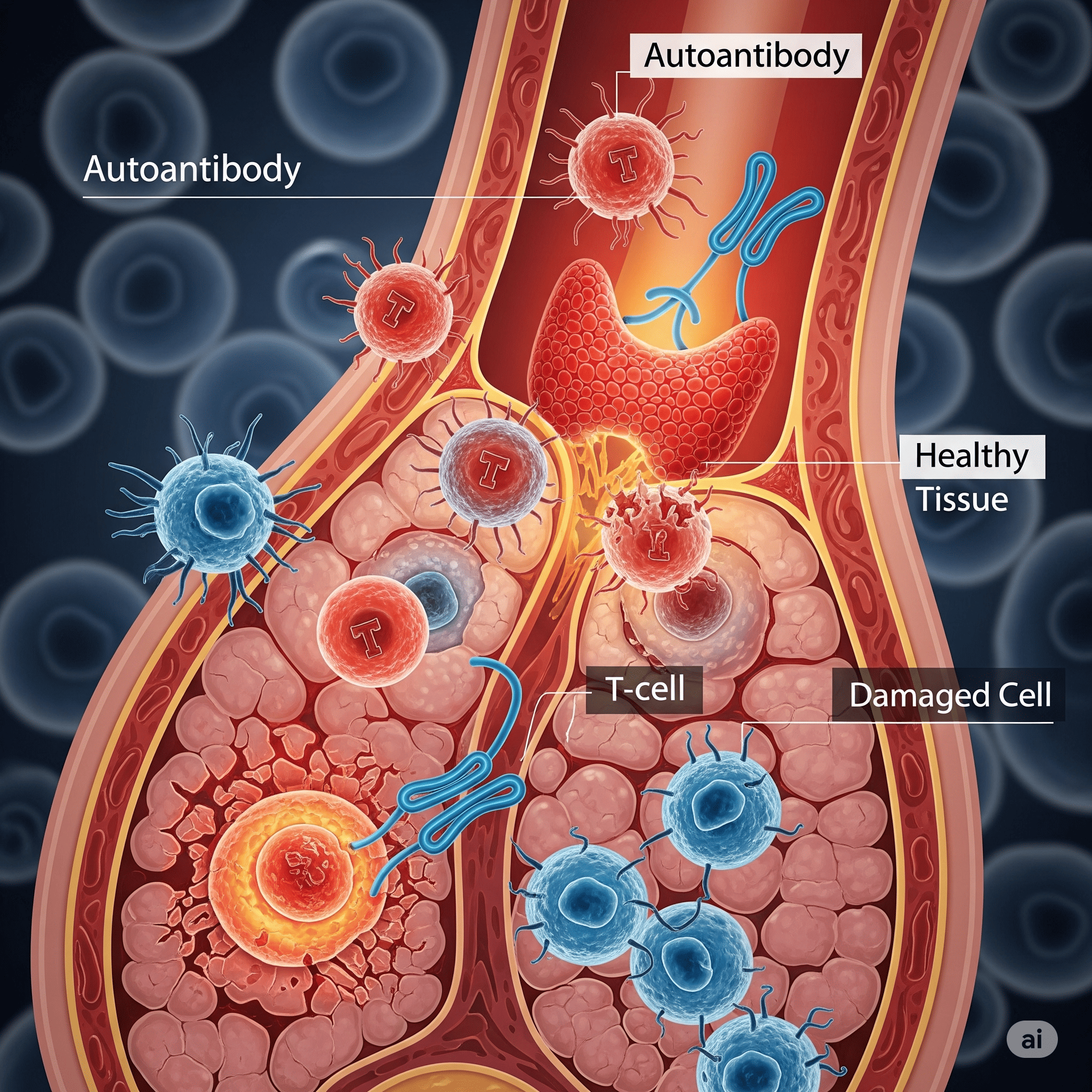
Uma doença autoimune é uma condição que se origina de uma reação imunitária anormal, na qual o corpo ataca uma parte normal de seu próprio organismo (autoimunidade). Em vez de combater invasores, o sistema imunológico identifica erroneamente células e tecidos saudáveis como ameaças e os ataca.
Prevalência: Não são tão raras como se pensa; um estudo recente da The Lancet indica que uma em cada 10 pessoas possui algum tipo de doença autoimune. Sua incidência e prevalência vêm crescendo.
Causas: Geralmente são de origem desconhecida e multifatoriais. Podem ser influenciadas por fatores:
Genéticos: Algumas doenças são familiares.
Ambientais: Infecções (ex: vírus Epstein-Barr), exposição à luz UV, tabagismo, obesidade, temperatura, e certos medicamentos podem desencadeá-las ou exacerbar.
Hormonais: Mais comuns em mulheres do que em homens (proporção 2:1 ou 3:1), muitas vezes iniciando na idade adulta ou entre a puberdade e a menopausa. Hormônios sexuais femininos são imunoestimulantes, enquanto os masculinos parecem ser imunossupressores.
Imunológicos: Disfunções no reconhecimento de "self".
Sintomas Comuns: Dependem da condição, mas incluem febre baixa e fadiga. Em muitos casos, os sintomas aparecem e desaparecem ciclicamente.
Órgãos Afetados: Podem acometer praticamente qualquer parte do corpo, desde um órgão único (como tireoidite de Hashimoto, doença celíaca, diabetes mellitus tipo 1, vitiligo) até serem sistêmicas, atingindo múltiplos órgãos e sistemas (como lúpus eritematoso sistêmico, artrite reumatoide).
Diagnóstico: Pode ser difícil, pois as manifestações são heterogêneas. Avanços como biomarcadores moleculares e testes de autoanticorpos permitem diagnósticos mais precisos e precoces.
Cura: Apesar dos tratamentos melhorarem os sintomas, geralmente não existe cura para as doenças autoimunes. Contudo, é possível estabilizar a doença e induzir remissão.
Avanços no Diagnóstico e Tratamento das Doenças Autoimunes
O tratamento das doenças autoimunes é complexo e depende do tipo e gravidade da condição. O objetivo principal é reduzir os danos, realinhar o sistema imune, estabilizar a doença e ajudar na remissão, além de melhorar a qualidade de vida dos pacientes.
1. Tratamentos Convencionais:
Tradicionalmente, incluem medicamentos que visam controlar a inflamação e suprimir o sistema imunológico de forma mais ampla:
Anti-inflamatórios Não Esteroides (AINEs): Reduzem a inflamação e aliviam sintomas como dor, mas não alteram a progressão da doença a longo prazo.
Analgésicos: Usados para controle da dor.
Corticosteroides: São os imunossupressores mais comuns e potentes, agindo na redução da produção de substâncias inflamatórias e na ação do sistema imunológico. Podem ter efeitos colaterais significativos com uso prolongado.
DMARDs (Fármacos Modificadores da Evolução da Doença Reumatismal): Retardam a progressão da doença, embora levem semanas ou meses para surtir efeito. Exemplos incluem metotrexato, hidroxicloroquina, sulfassalazina, azatioprina, leflunomida.
2. Medicamentos Biológicos (Biofármacos): A Revolução no Tratamento
Os medicamentos biológicos, ou biofármacos, representam um dos maiores avanços no tratamento das doenças autoimunes e reumáticas. Eles vieram revolucionar a indústria farmacêutica, oferecendo soluções para doenças que antes não eram eficazmente tratadas com terapias tradicionais.
O Que São? São fármacos obtidos ou derivados de organismos vivos (bactérias, leveduras, células de mamíferos), geralmente geneticamente modificados, por processos biotecnológicos. Ao contrário dos medicamentos sintéticos (químicos), que são moléculas pequenas e estáveis, os biológicos são moléculas grandes, muito complexas, instáveis e imunogênicas. Não é possível reproduzir cópias idênticas devido à complexidade de sua produção por sistemas vivos.
Como Funcionam? São projetados para atingir alvos celulares e moleculares específicos envolvidos na patogênese das doenças autoimunes. Isso resulta em uma ação mais direcionada e menos efeitos adversos em comparação com imunossupressores que atuam de forma mais ampla.
Vantagens: Melhoria significativa na qualidade de vida, restabelecimento de funções afetadas, prevenção de danos crônicos e recuperação funcional. Apresentam boa porcentagem de eficácia e segurança, geralmente sendo bem tolerados e com menor frequência de administração.
Desafios:
Custo Elevado: O acesso dos pacientes é muitas vezes limitado devido ao seu alto custo de desenvolvimento, produção e venda.
Instabilidade: Por serem proteínas, são suscetíveis à degradação química e física.
Imunogenicidade: Podem gerar uma resposta imune no organismo (produção de anticorpos contra o próprio biológico), o que pode inativar o medicamento e causar efeitos adversos.
Tempo de Semivida: São facilmente degradados por enzimas no organismo, o que levou ao desenvolvimento de modificações químicas para prolongar sua ação.
Risco de Infecções: Por serem potentes imunossupressores, aumentam o risco de infecções, pois diminuem a capacidade do sistema imunológico de combater microrganismos.
Contraindicações e Cuidados: Não recomendados durante a gravidez/amamentação, em casos de infecções ativas, câncer recente, doença desmielinizante, ou antes da administração de vacinas vivas. Requerem monitoramento médico regular.
3. Tipos e Mecanismos dos Medicamentos Biológicos (Exemplos Comuns):
A maioria das terapias biológicas visa citocinas, células B e moléculas de co-estimulação.
Anticorpos Monoclonais (mAbs): São anticorpos idênticos, específicos e puros que se ligam a um único epítopo (parte específica de um antígeno). Podem ser murinos (ratos), quiméricos (rato/humano), humanizados (maioria humano) ou totalmente humanos, para reduzir a imunogenicidade.
Anti-TNF-alfa (Fator de Necrose Tumoral alfa): O TNF-alfa é uma citocina pró-inflamatória crucial em muitas doenças autoimunes.
Adalimumabe (Humira®): IgG totalmente humana, bloqueia TNF-alfa. Usado em AR, psoríase, doença de Crohn, colite ulcerosa.
Infliximabe (Remicade®, Inflectra®): Anticorpo quimérico (IgG1), liga-se ao TNF-alfa solúvel. Usado em AR, psoríase, doença de Crohn, colite ulcerosa.
Golimumabe (Simponi®): Anticorpo monoclonal totalmente humano, neutraliza TNF-alfa. Usado em AR, colite ulcerosa.
Certolizumab pegol (Cimzia®): Anticorpo humanizado peguilado (com polietilenoglicol para maior tempo de vida e solubilidade), alta afinidade para TNF-alfa. Usado em AR, doença de Crohn.
Inibidores de Interleucinas (ILs):
Ustekinumabe (Stelara®): Anticorpo monoclonal que inibe IL-12 e IL-23 (citocinas importantes na psoríase e doença de Crohn). Usado em psoríase, doença de Crohn.
Tocilizumabe (Actemra®): Anticorpo monoclonal humanizado que neutraliza IL-6 (citocina inflamatória em AR) ao impedir sua ligação a receptores. Usado em AR.
Secucinumabe (Cosentyx®): Anticorpo monoclonal que se liga à IL-17A, bloqueando sua ação inflamatória. Usado em psoríase.
Ixecizumab (Taltz®): Anticorpo monoclonal que se liga à IL-17A. Usado em psoríase.
Brodalumabe (Siliq®): Anticorpo monoclonal que bloqueia a atividade das interleucinas 17 (A, F e A/F). Usado em psoríase.
Anakinra (Kineret®): Antagonista do receptor da interleucina 1 (IL-1). Usado em AR.
Sarilumab (Kevzara®): Anticorpo monoclonal que tem como alvo a IL-6, bloqueando sua ação. Usado em AR.
Bloqueadores de Células B:
Rituximabe (Rituxan®, MabThera®): Anticorpo monoclonal quimérico, direcionado contra a molécula CD20 na superfície dos linfócitos B, causando sua destruição. Usado em AR.
Belimumabe (Benlysta®): Anticorpo monoclonal humanizado que se liga à proteína BLyS (estimuladora de linfócitos B), inibindo sua atividade. Usado em lúpus eritematoso sistêmico (LES).
Bloqueadores da Co-estimulação de Células T:
Abatacept (Orencia®): Proteína de fusão humana (CTLA4 + porção Fc de IgG1), atua como inibidor seletivo de moléculas de co-estimulação, impedindo a ativação dos linfócitos T. Eficaz quando não há resposta a anti-TNF-alfa ou DMARDs. Usado em AR.
Bloqueadores de Moléculas de Adesão Celular:
Natalizumab (Tysabri®): Anticorpo recombinante humanizado, bloqueia a ação da integrina α4, impedindo a migração de leucócitos ativados para o sistema nervoso central e intestino. Usado em esclerose múltipla (EM), doença de Crohn.
Vedolizumab (Entyvio®): Anticorpo monoclonal humanizado que se liga especificamente à integrina α4β7, bloqueando a migração de leucócitos para o intestino. Usado em doença de Crohn, colite ulcerosa.
Proteínas de Fusão: Obtidas pela junção de uma imunoglobulina humana a um domínio proteico, por engenharia genética.
Etanercept (Enbrel®): Proteína de fusão (porção Fc de IgG humana + dois receptores solúveis do TNF-α), inativa a atividade biológica do TNF ligando-se a ele. Usado em AR, psoríase.
Interferons:
Interferon β 1-b e β 1-a: Reduzem a atividade inflamatória na esclerose múltipla (EM).
Outros:
Alemtuzumab (Lemtrada®): Anticorpo monoclonal que se liga à glicoproteína CD52 na superfície dos linfócitos B, destruindo-os. Usado em esclerose múltipla.
Daclizumab: Anticorpo que se liga a células do sistema imunitário, impedindo-as de atacar e danificar as células nervosas. Usado em esclerose múltipla. (Nota: Houve restrições de uso devido a eventos adversos hepáticos).
4. Medicamentos Biossimilares:
São versões "equivalentes" de medicamentos biológicos de referência, que surgem no mercado após a expiração da patente do biológico original. Embora não sejam cópias idênticas (como os genéricos são dos sintéticos) devido à complexidade de sua produção em sistemas vivos, são rigorosamente avaliados (qualidade, segurança, eficácia) por agências reguladoras como a EMA (Agência Europeia do Medicamento) para garantir que atuam da mesma forma para as mesmas patologias. Oferecem uma alternativa com custos mais acessíveis.
Principais Doenças Autoimunes e Seus Tratamentos Atuais (Detalhados)
Vamos aprofundar nas doenças autoimunes mais comuns e cobradas, detalhando seus tratamentos.
1. Artrite Reumatoide (AR):
O que é? Uma doença autoimune inflamatória crônica, a forma mais comum de artrite.
Acometimento: Afeta principalmente os punhos e dedos das mãos, mas pode atingir pés, ombros, joelhos, cotovelos, quadril e coluna vertebral, causando alterações em ossos, cartilagem e tendões. Ocasionalmente, pode afetar outros órgãos (coração, pulmões, olhos, pele), aumentando a morbidade.
Sintomas: Dor, rigidez matinal, fadiga e perda de peso. A prevalência aumenta com a idade e afeta 2-3 vezes mais mulheres que homens.
Mecanismo: Fatores genéticos, ambientais e imunológicos contribuem. A produção de autoanticorpos e a interação entre o sistema imune inato e adaptativo (células T CD4+, células B) são preponderantes. Citocinas pró-inflamatórias como TNF-alfa, IL-6, IL-1 e IL-17 desempenham papel crucial, levando a inflamação sinovial, efeitos sistêmicos (PCR elevada, doenças cardiovasculares, anemias, osteoporose) e destruição articular/óssea.
Tratamento Convencional:
Não farmacológico: Exercício, descanso equilibrado, alimentação adequada, cessação tabágica.
Farmacológico: AINEs (ibuprofeno, diclofenaco), analgésicos, corticosteroides (prednisona, prednisolona), DMARDs (hidroxicloroquina, metotrexato, sulfassalazina, azatioprina, leflunomida). O metotrexato é um DMARD frequentemente associado a biológicos.
Tratamento Biológico: Indicados para AR moderada a grave, reduzindo inflamação e progressão do dano articular. Mais eficazes em associação com metotrexato.
Inibidores do TNF-alfa:
Infliximabe: Anticorpo quimérico. Diminui erosões ósseas. Administrado IV. Risco de reações de infusão e infecções.
Adalimumabe: IgG totalmente humana. Menos imunogênico. Administrado SC a cada 14 dias. Efeitos adversos comuns: reação no local de aplicação, infecções.
Etanercept: Proteína de fusão. Inativa TNF-alfa, ligando-se a ele. Reduz inchaço, marcadores bioquímicos (ESR, PCR), rigidez e dor matinais. Administrado SC.
Certolizumab pegol: Anticorpo humanizado peguilado. Aumenta tempo de semivida. Reduz progressão de lesões. Administrado SC.
Golimumabe: Anticorpo totalmente humano. Neutraliza TNF-alfa. Administrado SC mensalmente.
Bloqueadores da Co-estimulação de Células T:
Abatacept: Proteína de fusão. Inibe a ativação de linfócitos T. Eficaz em casos sem resposta a anti-TNF-alfa ou DMARDs. Administrado IV.
Bloqueadores de Células B:
Rituximabe: Anticorpo quimérico anti-CD20. Usado em falha terapêutica com anti-TNF-alfa. Administrado IV. Reações infusionais comuns.
Inibidores da IL-6:
Tocilizumabe: Anticorpo humanizado. Neutraliza IL-6. Usado em AR moderada a grave. Administrado IV. Requer monitoramento sanguíneo regular devido a efeitos adversos como neutropenia, elevação de transaminases, colesterol.
Sarilumab: Anticorpo monoclonal que bloqueia IL-6. Usado em AR moderada a grave. Administrado SC.
Inibidor da IL-1:
Anakinra: Antagonista do receptor de IL-1. Usado em AR. Administrado SC. Menos eficaz que outros DMARDs biológicos.
Pesquisas em AR: Estudos clínicos no Brasil e em Portugal investigam a segurança e eficácia a longo prazo de biológicos (etanercept, upadacitinibe, sarilumab, sirukumab), buscando novas alternativas e melhores respostas.
2. Lúpus Eritematoso Sistêmico (LES):
O que é? Uma doença autoimune crônica e sistêmica, caracterizada por uma desregulação do sistema imunológico que leva à produção de uma ampla gama de autoanticorpos, principalmente contra antígenos nucleares.
Acometimento: Causa inflamação sistêmica que afeta diversos órgãos, incluindo pele, articulações, pulmões (pleura), coração (pericárdio), sistema nervoso central e rins. Pode se manifestar de diversas formas (lúpus discoide, induzido por medicamentos, neonatal, sistêmico).
Evolução: Varia de leve a grave, com momentos de agudização (surtos) e remissão, ou sintomas constantes. Afeta predominantemente mulheres (entre puberdade e menopausa), mas pode ocorrer em qualquer idade.
Mecanismo: Multifatorial, envolvendo fatores ambientais (luz UV, infecções como Epstein-Barr, medicamentos), hormonais, genéticos e imunológicos. Células T ativadas ajudam células B a produzir autoanticorpos.
Tratamento Convencional:
Não farmacológico: Diminuição da exposição solar (protetor solar), dieta equilibrada, redução do estresse, exercício físico, cessação tabágica.
Farmacológico: AINEs (para dor e inflamação), antimaláricos (cloroquina, hidroxicloroquina, usados em quase todos os pacientes), imunossupressores (azatioprina, ciclofosfamida, micofenolato mofetil – este último começou a ser distribuído no SUS –, metotrexato), corticosteroides (tópicos, intra-articulares, orais, IV para casos graves).
Tratamento Biológico: Desenvolvidas com o avanço do conhecimento da imunopatogênese.
Belimumabe (Benlysta®): Anticorpo monoclonal humanizado. Liga-se à proteína BLyS (estimuladora de linfócitos B), inibindo sua atividade e a sobrevivência das células B. Usado em LES leve a moderado em adultos. Administrado IV. Efeitos adversos: infecções do trato respiratório, náuseas, diarreia, cefaleias.
Novidade: Novo tratamento para lúpus com células T CAR (Car-T cell therapy) promete acabar com a necessidade de remédios em alguns casos, demonstrando resultados promissores.
Pesquisas em LES: Estudos clínicos em Portugal investigam segurança e eficácia de belimumabe (redução do uso de corticosteroides) e ALX-0061 (vobarilizumabe).
3. Psoríase:
O que é? Uma doença inflamatória crônica de origem imunológica, não contagiosa. Caracterizada por crescimento e diferenciação excessivos dos queratinócitos, levando a inflamação, espessamento e descamação da pele.
Prevalência: Afeta 2-3% da população mundial, com variações geográficas. Em Portugal, cerca de 250 mil pessoas. Pode surgir em qualquer idade, com picos em adultos jovens e após os 40 anos, afetando ambos os sexos.
Formas de Manifestação: Mais comum é a psoríase em placas (85-90% dos casos), caracterizada por lesões avermelhadas, descamativas e elevadas, principalmente em cotovelos, joelhos, couro cabeludo. Outros tipos: gutata, eritrodérmica, inversa, palmoplantar, pustulosa. Alguns pacientes desenvolvem artrite psoriática.
Mecanismo: Fatores genéticos (36-91% de probabilidade em famílias com a doença), ambientais (álcool, tabagismo, obesidade, infecções) e imunológicos. A interação entre células dendríticas e células T (TH1, TH17) com múltiplas citocinas e fatores de crescimento é responsável pela hiperplasia epidérmica e inflamação. Pode ser exacerbada por AINEs, lítio, antimaláricos.
Tratamento Convencional:
Não farmacológico: Emolientes, hidratantes, agentes queratolíticos; redução do estresse, exercício, alimentação equilibrada, redução de tabaco/álcool.
Farmacológico:
Tópicos: Corticosteroides, análogos da vitamina D3 (calcipotriol), retinoides (tazaroteno), antralina, alcatrão da hulha, ácido salicílico. Usados em casos leves a moderados.
Fototerapia: Radiação UVA e UVB para tratar lesões.
Sistêmicos (tradicionais): Ciclosporina e metotrexato (imunossupressores). Acitretina (análogo do ácido retinoico) para formas graves.
Tratamento Biológico: Alta eficácia na psoríase em placas moderada a grave, bom perfil de segurança e tolerabilidade.
Ustekinumabe: Anticorpo monoclonal, inibe diferenciação de linfócitos T ao ligar-se a IL-12 e IL-23. Administrado SC. Contraindicado com vacinas vivas.
Secucinumabe: Anticorpo monoclonal que se liga à IL-17A, bloqueando sua ação inflamatória. Administrado SC. Não em infecções ativas.
Ixecizumab: Anticorpo monoclonal que se liga à IL-17A. Administrado SC.
Adalimumabe: (já descrito em AR) Usado em psoríase crônica em placas, inclusive em crianças e adolescentes.
Infliximabe: (já descrito em AR) Indicado para psoríase em placas moderada a grave que não responde a outras terapias.
Etanercept: (já descrito em AR) Usado em psoríase em placas moderada a grave refratária.
Brodalumabe: Anticorpo monoclonal que bloqueia a atividade das interleucinas 17 (A, F e A/F). Administrado SC. Contraindicado em doença de Crohn ativa e infecções. Relatos de comportamentos suicidas.
Pesquisas em Psoríase: Estudos detalham a segurança do infliximabe e ustecinumabe, e avaliam a segurança e eficácia do etanercept em psoríase pediátrica.
4. Esclerose Múltipla (EM):
O que é? Uma doença degenerativa, inflamatória crônica, na qual o sistema imunológico ataca o sistema nervoso central (cérebro, medula espinal e nervos ópticos), atingindo a mielina e as fibras nervosas. O termo "esclerose" refere-se à cicatrização da mielina danificada.
Sintomas: Fadiga, neurite óptica, perda de força muscular, alterações de sensibilidade, dor, problemas urinários/intestinais, sexuais, de equilíbrio/coordenação, cognitivos e depressão.
Formas de Manifestação: Esclerose múltipla surto-remissão (mais comum, com períodos de surtos e remissão), secundária progressiva, primária progressiva e benigna.
Epidemiologia: Duas vezes mais comum em mulheres, diagnosticada entre 20-50 anos, rara em crianças/idosos. Mais frequente em zonas distantes do equador (Europa, América do Norte) e em pessoas de raça branca.
Mecanismo: Pensa-se em tendência hereditária e combinação de fatores diversos. Não há prova segura de vírus específico, mas a hipótese de um vírus contraído na infância é considerada.
Tratamento Convencional:
Terapia Sintomática: Para manter a qualidade de vida.
Tratamento de Crises Agudas: Corticosteroides IV (metilprednisolona) para diminuir severidade e duração dos sintomas.
Terapia Modificadora da Doença: Para modificar o curso da doença e diminuir a progressão das incapacidades.
Acetato de glatirâmero: Polipeptídeo sintético, usado em casos de reincidências. Mimetiza propriedades antigênicas da proteína básica de mielina (MBP).
Não farmacológico: Estilo de vida saudável (exercício, alimentação, não fumar), níveis adequados de vitamina D.
Tratamento Biológico:
Interferon β 1-b e β 1-a: Reduzem a atividade inflamatória. Administrados SC ou IM. Indicados em surtos e remissões.
Natalizumab: Anticorpo recombinante humanizado. Bloqueia a integrina α4 (β1 e β7), impedindo migração de leucócitos para o SNC. Administrado IV. Risco de leucoencefalopatia multifocal progressiva (infecção oportunista fatal).
Alemtuzumab: Anticorpo monoclonal. Liga-se à glicoproteína CD52 na superfície dos linfócitos B, destruindo-os. Usado em EM surto-remissão ativa.
Daclizumab: Anticorpo que se liga a células do sistema imunitário. Usado em EM. (Nota: Houve restrições e revisão de segurança devido a danos hepáticos).
Pesquisas em EM: Estudos clínicos em Portugal avaliam a eficácia e segurança de ocrelizumabe (em EM recidivante e progressiva primária) e ofatumumabe, e o impacto a longo prazo do natalizumabe.
5. Doença de Crohn (DC):
O que é? Uma doença inflamatória crônica, transmural (afeta todas as camadas da parede intestinal) e recidivante, que pode ocorrer em qualquer parte do trato digestivo (boca ao ânus), mas mais comum no íleo e intestino grosso. O acometimento é segmentar, com áreas saudáveis entre os segmentos inflamados.
Sintomas: Diarreia (às vezes com sangue), perda de apetite e peso. Complicações: oclusão intestinal, úlceras, fístulas.
Epidemiologia: Mais comum antes dos 30 anos (14-24 anos), maior incidência no sexo feminino. Mais comum em áreas urbanas de países industrializados.
Mecanismo: Causa desconhecida. Provável que um vírus ou bactéria leve a uma resposta imunológica exagerada, causando inflamação. Fatores genéticos e hereditários estão relacionados.
Tratamento Convencional:
Objetivos: Melhoria da qualidade de vida, preservação da função intestinal, prevenção de complicações.
Medicamentos: Antidiarreicos (difenoxilato, loperamida), anti-inflamatórios (sulfassalazina, mesalazina), imunomoduladores (azatioprina, mercaptopurina, metotrexato, ciclosporina – esta para fístulas). Corticosteroides para crises agudas.
Antibióticos: Para abscessos e fístulas perianais.
Cirurgia: Necessária em alguns casos (oclusão intestinal, fístulas, episódios agudos graves).
Não farmacológico: Alimentação equilibrada, variada e saudável (pacientes podem ter deficiências nutricionais).
Tratamento Biológico: Usados em DC moderada a severa, para induzir e manter remissão quando a terapia convencional é inadequada ou intolerada.
Anti-TNF-alfa:
Infliximabe: (já descrito) Indicado para DC ativa moderada a grave em adultos, crianças e adolescentes (6-17 anos). Usado em associação com imunossupressores.
Adalimumabe: (já descrito) Indicado para DC em pacientes pediátricos (>6 anos) e adultos.
Inibidores da Integrina:
Vedolizumab: Anticorpo monoclonal humanizado. Liga-se à integrina α4β7, bloqueando a migração de leucócitos para o endotélio intestinal. Usado em casos de ineficácia ou intolerância a terapias convencionais ou anti-TNF-alfa.
Inibidores de Citocinas:
Ustekinumabe: (já descrito) Inibe IL-12 e IL-23. Usado em DC ativa moderada a grave.
Pesquisas em DC: Estudos clínicos em provocando úlceras e sangramento.
Sintomas: Diarreia com sangue e muco, dor abdominal, urgência retal. Casos graves podem incluir febre, perda de peso e fadiga.
Epidemiologia: Afeta ambos os sexos, geralmente surge entre 15-40 anos e 50-80 anos.
Mecanismo: Desconhecido, mas acredita-se em uma resposta imunológica exagerada contra a microflora intestinal normal. Fatores de risco incluem idade, história familiar e hereditariedade. Estresse pode agravar os sintomas.
Tratamento Convencional:
Não há cura definitiva, o tratamento visa o controle dos sintomas.
Medicamentos: Anti-inflamatórios (sulfassalazina, olsalazina, mesalamina, balsalazida) para inflamação e manutenção da remissão.
Imunomoduladores: Azatioprina, mercaptopurina (para remissão a longo prazo), ciclosporina (para crises agudas não responsivas a corticosteroides).
Suplementos de ferro para anemia.
Cirurgia: Para casos graves, muito frequentes ou com alto risco de malignização.
Tratamento Biológico:
Infliximabe: (já descrito) Usado em CU ativa moderada a grave que não respondeu à terapia convencional.
Vedolizumab: (já descrito) Usado em CU ativa moderada a grave em casos de ineficácia ou intolerância a terapias convencionais ou anti-TNF-alfa.
Adalimumabe: (já descrito) Usado em CU.
Golimumabe: (já descrito) Usado em CU ativa moderada a grave.
Pesquisas em CU: Estudos em Portugal investigam a segurança e eficácia de etrolizumabe, e comparam vedolizumabe IV com adalimumabe SC.
Perspectivas Futuras e Pesquisas em Autoimunidade
A pesquisa contínua e a aplicação de novas tecnologias são cruciais para o avanço no tratamento das doenças autoimunes.
Biomarcadores Moleculares: Permitem diagnósticos mais precisos e precoces.
Pesquisa Genética e Microbiota Intestinal: São particularmente promissoras para o desenvolvimento de tratamentos mais personalizados e direcionados. A modulação da microbiota intestinal é uma estratégia assertiva para realinhar o sistema imune e pode prevenir o aparecimento de novas doenças autoimunes.
Terapias Biológicas e Regenerativas: O uso de células-tronco tem mostrado resultados promissores em alguns casos.
Modulação Imunológica: Há pesquisas focadas em treinar subconjuntos de células para corrigir a resposta imunológica exagerada. A identificação de enzimas como a PRMT5 é um exemplo nesse sentido.
Foco na Cura: Embora ainda não haja grandes perspectivas para a cura de muitas condições autoimunes, o objetivo é diminuir a quantidade de células autorreativas para bloquear a progressão da doença.
Papel do Timo: Novas descobertas sobre a função das células B no timo, educando as células T para não atacarem os tecidos corporais, abrem novas vias para tratamentos direcionados.
Ensaios Clínicos: Portugal, como outros países, participa ativamente de diversos ensaios clínicos com medicamentos biológicos, buscando mais informações sobre fármacos existentes, comparando resultados e estudando novos medicamentos para maior segurança e eficácia.
Cuidados e Qualidade de Vida para Pacientes com Doenças Autoimunes
Além dos tratamentos medicamentosos, a adoção de um estilo de vida saudável é um pilar fundamental para pacientes com doenças autoimunes.
Alimentação: Realinhar o sistema imune através da modulação da microbiota intestinal é crucial. A adesão à dieta mediterrânea, acompanhada de suplementações individualizadas (magnésio, ômega 3, vitamina D, probióticos, própolis), pode reduzir danos e prevenir novas doenças. É essencial remover "gatilhos agressores" da alimentação para melhor qualidade de vida.
Controle de Gatilhos: Identificar e controlar gatilhos externos e internos que possam aprofundar a doença autoimune.
Cuidado Integrativo: Envolve o controle das emoções, ligação com a espiritualidade, prática de esportes, ioga e meditação.
Higiene: Lavar as mãos frequentemente, evitar contato com pessoas doentes, evitar ambientes fechados e tocar no rosto.
Sono: Dormir pelo menos 8 horas por noite.
Atividade Física: Praticar regularmente, conforme orientação médica.
Um Futuro Promissor com Desafios Constantes
As doenças autoimunes representam um desafio complexo para a saúde global, afetando milhões de pessoas e exigindo uma compreensão aprofundada de seus mecanismos. A evolução do conhecimento sobre a patogênese dessas condições, aliada aos avanços da biotecnologia e da engenharia genética, impulsionou o desenvolvimento de medicamentos biológicos que revolucionaram o tratamento e o prognóstico para os pacientes.
Apesar do alto custo e dos desafios relacionados à estabilidade e imunogenicidade, o mercado de biofármacos continua em expansão, impulsionado pela alta eficácia e pela capacidade de transformar a história natural de muitas doenças. A busca por diagnósticos precoces e terapias personalizadas, incluindo a modulação da microbiota e a terapia com células T CAR, demonstra o potencial transformador da medicina atual.
É fundamental que a pesquisa continue avançando e que políticas de saúde inclusivas garantam o acesso universal a esses avanços médicos, promovendo uma abordagem equitativa no cuidado a essas condições complexas. O futuro no manejo das doenças autoimunes afigura-se positivo, com a promessa de novas melhorias e uma qualidade de vida cada vez melhor para os pacientes. Compreender esses mecanismos e tratamentos é essencial para todos que buscam excelência na área da saúde e em suas jornadas acadêmicas e profissionais.
Lista de Exercícios:
Questão 1:
O que caracteriza as doenças autoimunes?
a) Ataques do sistema imunológico às células estranhas ao organismo.
b) Falha do sistema imunológico em atacar células e tecidos saudáveis do próprio organismo.
c) Produção de anticorpos específicos para o antígeno.
d) Uso de medicamentos para estimular o sistema imunológico.
Questão 2:
Quais são alguns exemplos de doenças autoimunes?
a) Hipertensão e diabetes tipo 2.
b) Asma e bronquite.
c) Lúpus eritematoso sistêmico e esclerose múltipla.
d) Catarata e glaucoma.
Questão 3:
Qual é o objetivo principal do tratamento para doenças autoimunes?
a) Estimular a produção de autoanticorpos.
b) Reduzir a atividade do sistema imunológico e controlar a inflamação.
c) Aumentar a respostsa imune primária.
d) Prevenir a memória imunológica.
Gabarito:
b) Falha do sistema imunológico em atacar células e tecidos saudáveis do próprio organismo.
c) Lúpus eritematoso sistêmico e esclerose múltipla.
b) Reduzir a atividade do sistema imunológico e controlar a inflamação.